Inteligencia Artificial y el futuro incierto de los antibióticos
Por Faustino Gijón Hernández
Vivimos una época fascinante y alarmante
La medicina, bastión del ingenio humano que en el siglo XX domó infecciones que antes diezmaban poblaciones enteras, hoy parece perder terreno. Las bacterias, en su silenciosa evolución, se nos escapan de las manos. ¿Volveremos a un tiempo en que una herida menor podía costar la vida? ¿Será posible que, en pleno siglo XXI, debamos enfrentar un escenario posantibióticos?

IA: la nueva brújula de la farmacología
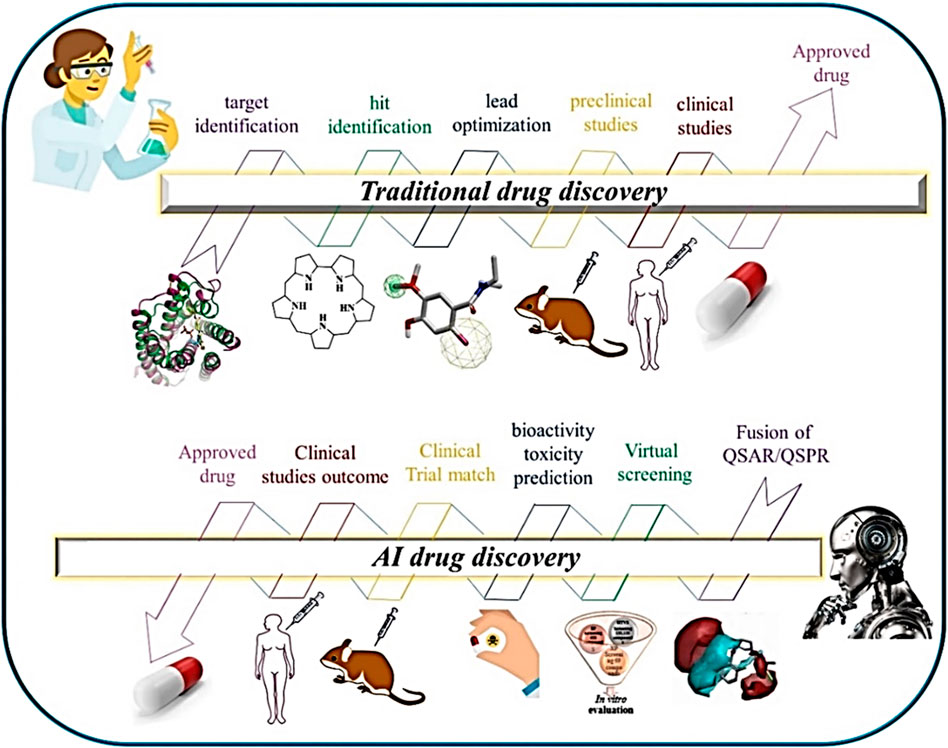
La inteligencia artificial (IA) ha abierto rutas insospechadas: cribado virtual de millones de moléculas, diseño de compuestos inéditos mediante modelos generativos, y predicción de resistencia antes de que surja en los hospitales. Promete acelerar lo que antes tomaba décadas, sin eximirnos del veredicto final de la biología: permeabilidad, toxicidad, farmacocinética. No es casualidad que el Nobel de Química 2024 recayera en quienes demostraron el poder de la IA y la computación para desentrañar la arquitectura de las proteínas (nobelprize.org; El País), un hito que no sólo transformó la biología estructural, sino que también envió un mensaje inequívoco: el futuro del descubrimiento biomédico estará marcado por la integración entre algoritmos, datos y creatividad científica.
Ciencia sin economía es ciencia incompleta
Los antibióticos se recetan por pocos días y, si son efectivos, se usan lo menos posible para evitar resistencia. El retorno económico es pobre y varias compañías han abandonado el campo (Årdal et al., 2023; Shlaes, 2024). No es sólo un problema técnico: hay un desajuste entre interés público y lógica de mercado.
Nuevos modelos para un bien común
Algunas naciones ensayan soluciones: el modelo de suscripción en el Reino Unido (“Netflix de antibióticos”) y la propuesta PASTEUR Act en EE. UU. buscan desacoplar el valor del antibiótico del volumen de ventas (NHS England, 2022; Outterson et al., 2022).
A ello se suman iniciativas europeas como la Alianza Global contra la Resistencia a los Antibióticos (GARDP), que impulsa colaboraciones público-privadas para garantizar el acceso a nuevos compuestos esenciales, y propuestas de “market entry rewards”, en las que los Estados ofrecen incentivos económicos sustanciales a las farmacéuticas que logren introducir antibióticos verdaderamente innovadores. El esquema que se muestra a continuación (en inglés) sintetiza la lógica: el pago se otorga por el valor clínico y la necesidad pública de un nuevo antibiótico —no por el volumen de ventas—, a cambio de compromisos de acceso y uso responsable.

El desafío mexicano: entre urgencias y oportunidades
En México, la resistencia antimicrobiana no es una amenaza futura: ya está aquí. La Red PUCRA (UNAM) analizó más de 41 000 aislamientos de bacteriemias en hospitales de 15 estados; tres de cada cuatro fueron bacterias gramnegativas. En algunos centros, los aislamientos XDR crecieron del 5 % (2021) al 21 % (2023) (PUCRA, 2024). En ciertos hospitales, MRSA alcanza 85.7 % y E. coli muestra resistencias cercanas al 67 % en ITU (Rivera et al., 2021). También se han reportado brotes de Klebsiella oxytoca multidrogo resistente con mortalidad elevada (El País, 2024).
El uso irracional de antibióticos agrava el problema: hasta 80 % de pacientes con IRAS reciben antibióticos, aunque la mayoría de estos cuadros son virales (Cabello et al., 2008).
Lo que urge cambiar
- Infraestructura nacional de cómputo accesible para proyectos biomédicos.
- Bases de datos de resistencia representativas de cepas mexicanas (protocolos estandarizados).
- Convocatorias SECIHTI para IA aplicada a salud con validación experimental.
- Reconocer el acceso a nuevos antibióticos como prioridad de seguridad nacional.
¿Estamos a la altura del desafío?
La IA nos da herramientas formidables, pero no sustituye voluntad política ni responsabilidad colectiva. Los antibióticos son un bien común: una póliza de seguro para el futuro. Si queremos que los hallazgos crucen el umbral del laboratorio hacia hospitales y comunidades, tendremos que redefinir incentivos, exigir políticas visionarias y asumir que la salud futura se decide en el presente.
Referencias
- Årdal, C., Outterson, K., & Røttingen, J. A. (2023). Strengthening the antibiotic pipeline: economic and policy solutions. Nature Reviews Drug Discovery, 22, 75–88.
- Cabello, F., et al. (2008). Uso inadecuado de antibióticos en IRAS y EDAS en México. Salud Pública de México, 50(6), 481–488.
- El País. (2024, diciembre 7). Comun es hospitales… brote de Klebsiella oxytoca.
- NHS England. (2022). Antibiotic subscription model pilot evaluation report.
- Outterson, K., et al. (2022). The PASTEUR Act: a bold step for antibiotic market reform. Health Affairs Blog.
- PUCRA. (2024). Informe anual de resistencia antimicrobiana. UNAM.
- Rivera, J. et al. (2021). Prevalencia de resistencias en Enterobacteriaceae en hospitales mexicanos.
